看見更快的癒合力:人體細胞證實 PDL® 雷射表面可主動啟動「血管新生」
國防醫學院 2025 最新研究:揭開植體早期骨整合的關鍵生物機制
- 主動誘發癒合: 證實 PDL® 表面不只是物理粗糙化,更能作為「生物訊號」主動命令細胞長出血管。
- 男女皆有效: 首次發現植體對不同性別有精細的活化路徑差異(男性啟動 CCN1、女性啟動 EDIL3),但最終皆能促進血管網生成,顯示高度生物適應性。
- 臨床實證支持: 在先進的 3D 類器官模型中,PDL® 組別生成的微血管長度與密度皆顯著優於傳統 SLA 表面。
植牙成功的關鍵往往取決於最初幾週。國防醫學院與陽明交通大學研究團隊發表於權威期刊 Journal of Dental Sciences (2025) 的最新研究證實:Biomate PDL® 雷射微米通道表面,能顯著提升牙齦間質幹細胞(GMSC)的活性,加速植體周圍「血管新生」(Angiogenesis)。這意味著能更快為新生骨組織帶來氧氣與營養,是實現早期骨整合的關鍵一步。
充足的微血管供應就像是工地的後勤補給線,對於植體早期的穩定度至關重要。PDL® 表面能更早啟動這一過程,有助於:
- 更快的初期癒合: 提供骨修復所需的氧氣與營養,縮短等待期。
- 更強的軟組織封閉: 建立健康的牙齦袖口,減少細菌入侵機會。
- 更可預期的骨整合: 即使在骨質條件普通的案例中,也能提供穩定的生物學基礎。
證據一:不只是植體,更是細胞的「導航員」
研究比較了三種鈦表面:機械加工面、傳統 SLA、以及 Biomate PDL® 雷射微通道面。電子顯微鏡下的結果令人驚艷:PDL® 表面的微米級溝槽就像是細胞的「導航跑道」。

這種獨特的物理結構提供了最佳的細胞附著環境,為後續的生物學反應奠定了良好基礎。
證據二:啟動「血管新生」的基因開關
這項研究最突破性的發現在於,PDL® 表面並非被動等待癒合,而是能主動調控細胞基因。研究團隊利用先進的基因定序技術發現,接觸到 PDL® 表面的幹細胞,其負責血管新生的關鍵基因——CCN1 與 EDIL3——表現量顯著提升。
簡單來說,這些幹細胞就像是被 PDL® 表面「喚醒」了,開始釋放裝滿 CCN1 與 EDIL3 信號分子的「傳令兵」(細胞外囊泡 EVs),呼叫周邊的血管內皮細胞過來集合、構築新的血管網。
? 發現:因應生理性別的精準修復
研究還有一個有趣的發現:人體細胞對植體表面會產生「男女有別」的細緻反應。
- 男性細胞:主要透過 CCN1 路徑活化。
- 女性細胞:則傾向使用 EDIL3 路徑。
但重點是,殊途同歸——無論性別,PDL® 表面最終都能成功啟動血管新生機制,證明了該技術具有高度的生物適應性。
證據三:3D 模型親眼見證血管網生成
為了模擬真實人體環境,研究團隊建立了先進的「3D 血管生成類器官模型」。結果直觀地顯示,在 Biomate PDL® 植體周圍,長出了最茂密、最完整的微血管網絡。
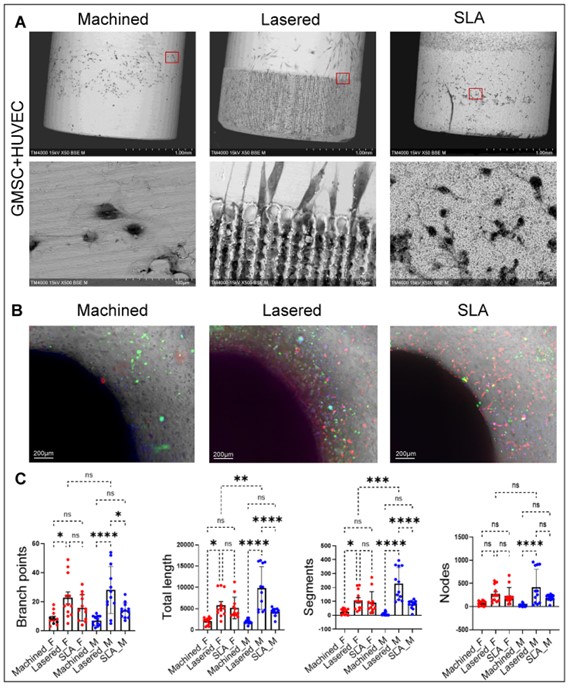
這項實驗強力證實:PDL® 表面技術能有效在植體植入初期,加速建立關鍵的血液供應系統。
結論:科學實證的安心選擇
這項由國防醫學院與陽明交通大學進行的嚴謹研究,從細胞分子層次到 3D 組織模型,全面解析了 Biomate PDL® 雷射微米通道表面促進早期癒合的生物機制。選擇 PDL®,就是選擇一個經過科學驗證、能主動促進血管新生與骨整合的先進植體系統。
原始研究來源:
Laser-modified titanium surfaces induce sex-dimorphic secretion of angiogenic factors by gingiva-derived mesenchymal stromal cells. Journal of Dental Sciences (2025).
前往閱讀 DOI 全文 >

